Perbedaan unsur dan senyawa seringkali disalahpahami oleh orang awam, terutama anak-anak di bangku sekolah yang baru belajar kimia. Mungkin ketiga istilah tersebut sudah sering kalian dengar, baik itu di sekolah ataupun di luar sekolah. Tapi apa sih sebenarnya pengertian dan perbedaan dari ketiganya? Kita akan sibak sebagai berikut dimulai dari pengertian unsur.
Untuk kamu yang ingin langsung ke perbedaan, bisa loncat ke bagian C ya!
Daftar Isi
A. Pengertian Unsur
Unsur adalah zat yang tidak dapat uraikan lagi menjadi zat yang lebih sederhana melalui reaksi kimia biasa. Unsur adalah zat penyusun dasar semua materi di alam semesta.
Contoh unsur adalah, hidrogen, helium, lithium, oksigen, karbon, emas, merkuri, dan lain sebagainya.
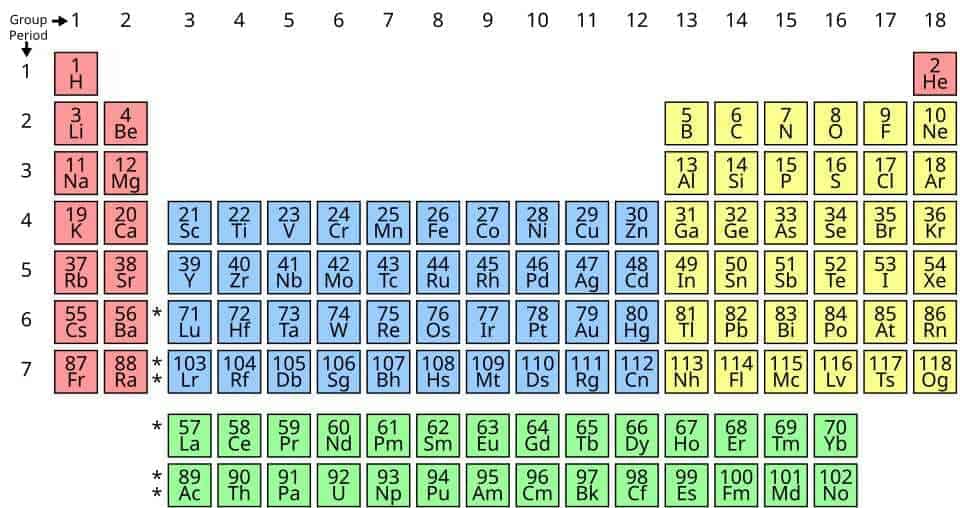
Sejauh ini, sudah ditemukan sebanyak 118 unsur kimia. Meskipun sudah sebanyak itu, para ilmuwan tetap berusaha untuk menciptakan elemen yang lebih berat lagi seperti elemen ke 119 dan 120.
118 elemen yang sudah ditemukan keseluruhannya dituangkan dalam tabel periodik sebagai berikut.
Semua materi di alam semesta kita ini pasti tersusun dari atom-atom yang merupakan bentuk dari suatu unsur. Unsur kimia tersebut dapat ditemukan baik dalam bentuk tunggal (murni) ataupun dalam bentuk molekul dan senyawa.
Unsur dalam bentuk murni artinya suatu zat tersebut hanya tersusun atas atom-atom unsur tersebut.
Baca juga: Sifat-Sifat Unsur Golongan Utama di Alam
Seperti yang dituangkan dalam tabel periodik di atas, setiap unsur memiliki simbolnya masing-masing. Simbol ini terdiri atas satu, dua, atau tiga huruf yang biasanya merupakan singkatan dari namanya (kadang nama latinnya). Misalnya simbol dari karbon, hidrogen, dan oksigen adalah C, H, dan O. Ssedangkan simbol dari besi adalah Fe yang berasal dari nama latinnya ferrum.
Itu adalah sekilas mengenai unsur, berikutnya mari kita pahami senyawa.
B. Pengertian Senyawa
Senyawa adalah zat tunggal yang tersusun atas dua atau lebih unsur kimia yang saling berikatan dengan ikatan kimia. Senyawa adalah zat tunggal yang tersusun dari beberapa unsur dengan perbandingan massa tetap.
Contoh senyawa adalah air (H2O), metana (CH4), garam dapur (NaCl), glukosa (C6H12O6), dan lain sebagainya.
Pada dasarnya, senyawa merupakan gabungan atom-atom suatu senyawa yang saling berikatan yang membentuk zat baru. Kombinasi atom-atom unsur yang berbeda menghasilkan senyawa yang berbeda pula.
Pada contoh di atas, ikatan antara atom hidrogen dan atom karbon membentuk senyawa air, ikatan antara atom natrium dan atom klorin membentuk senyawa garam dapur, dan ikatan antara atom, atom hidrogen, atom oksigen membentuk senyawa glukosa.
Maka dari itu, kita dapat mengetahui atom-atom apa saja yang terlibat dalam suatu senyawa dengan melihat simbol senyawa tersebut.
Sama halnya seperti dalam pembacaan simbol atau notasi suatu unsur. Dalam senyawa, huruf menyatakan unsur-unsur apa saja yang berikatan dalam senyawa tersebut. Sedangkan angka di kanan bawah setiap simbol unsur mewakili jumlah atom unsur tersebut dalam 1 senyawa.
Contohnya adalah misalnya senyawa air (H2O). Notasi H2O dapat menyatakan bahwa tiap 1 senyawa ini tersusun atas 2 atom hidrogen dan 1 atom oksigen.
C. Perbedaan Unsur dan Senyawa
Perbedaan unsur dan senyawa adalah bahwa unsur adalah zat dasar suatu materi dan hanya tersusun atas satu jenis atom sedangkan senyawa adalah suatu zat yang tersusun atas dua atau lebih unsur dan tersusun atas dua atau lebih atom yang berbeda.
Jadi, unsur dan senyawa sama-sama merupakan suatu zat namun unsur dan senyawa berbeda dari segi jumlah unsur dan macam atomnya. Jika zat tersebut hanya tersusun dari satu jenis arom alias satu unsur, maka itulah unsur. Jika zat tersebut tersusun dari dua atau lebih jenis atom yang saling berikatan, maka itu disebut senyawa.
Contohnya adalah zat yang hanya terdiri dari atom oksigen adalah suatu unsur, yakni unsur oksigen, dilambangkan dengan H. Namun jika atom-atom oksigen tersebut beraksi dan berikatan dengan atom-atom hidrogen membentuk H2O ataupun H2O2, maka akan terbentuk suatu senyawa, yakni air (H2O) dan dihidrogen peroksida (H2O2).
Referensi:
